
Нормативная лексика марта 2026: Что изменилось для рынка медизделий.
Март 2026 года преподнес сразу несколько знаковых решений, которые меняют ландшафт для производителей, импортеров и даже разработчиков медицинского софта. Пока все следили за продлением эксперимента по маркировке, регуляторы подготовили «сюрпризы» в виде бессрочного ввоза по жизненным показаниям, нового фармаконадзора для МИ и проекта закона об ИИ.
В этом обзоре — только ключевые изменения для отрасли здравоохранения со сроками и конкретными действиями.
Маркировка медизделий: Эксперимент продлен до февраля 2027 года (Постановление № 204)
Правительство РФ 28 февраля 2026 года продлило эксперимент по маркировке. Новый срок окончания — 28 февраля 2027 года.
Главное нововведение — поэтапная структура:
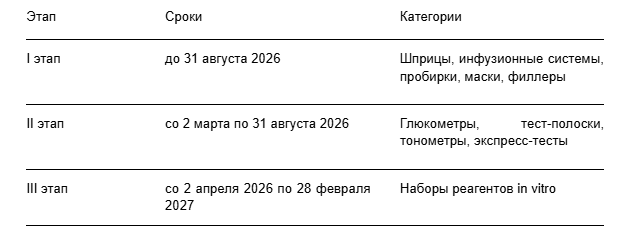
Важный нюанс: коды маркировки оператор (ЦРПТ) предоставляет бесплатно только в период проведения соответствующего этапа. Как только этап заканчивается — коды становятся платными.
Почему продлили: отрасль столкнулась с техническими сложностями при нанесении кодов «Честный знак» на разные виды упаковки и обеспечением их считываемости в течение требуемого срока.
Что делать сейчас:
Если ваше изделие в списке I–III этапов — срочно регистрироваться в системе «Честный ЗНАК».
Отрабатывать интеграцию именно в период своего этапа, пока коды бесплатны и ошибки не критичны.
Ввоз МИ по жизненным показаниям: разрешения могут стать бессрочными (проект изменений в ПП № 1590)
Минздрав подготовил проект, который отменяет 30-дневное ограничение срока действия разрешений на ввоз медизделий по жизненным показаниям.
Что изменится:
Разрешение станет бессрочным — не нужно будет переподавать документы из-за логистических, платежных или производственных задержек.
Срок рассмотрения заявки Росздравнадзором увеличится с 3 до 4 рабочих дней.
Уведомление о результате будет направляться в личный кабинет на Госуслугах (электронный формат).
Для бизнеса: значительное упрощение импорта редких и экстренных изделий. Особенно актуально для пациентоориентированных компаний, работающих с орфанными заболеваниями.
Фармаконадзор для медизделий: новые порядки с 1 сентября 2026 (два проекта приказов Минздрава)
Минздрав предложил полностью обновить систему мониторинга безопасности МИ. Общественное обсуждение проектов шло до 31 марта 2026 года. Вступление в силу — 1 сентября 2026 года (будут действовать до 1 сентября 2032 года).
Ключевые изменения:
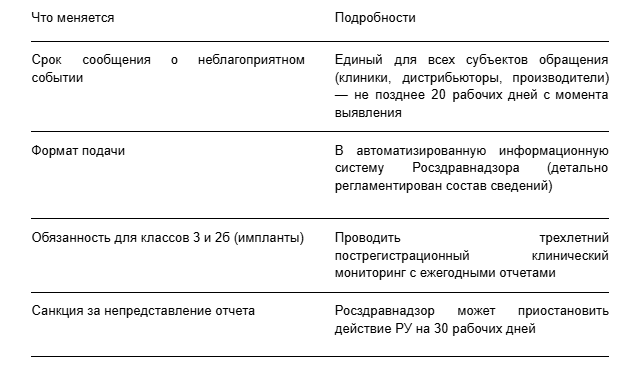
Что делать сейчас: Начинайте выстраивать внутренние процессы сбора и подачи данных в АИС Росздравнадзора. 20 рабочих дней — очень короткий срок для клинической организации.
Закон о русском языке: требования распространяются на сайты и интернет-магазины (разъяснения Роспотребнадзора от 2 марта 2026)
В связи со вступлением в силу статьи 10.1 Закона о защите прав потребителей, Роспотребнадзор выпустил руководство по соблюдению обязательных требований.
Что важно для участников рынка медизделий:
Требование использовать русский язык распространяется не только на вывески и упаковку, но и на сайты и страницы в интернете.
Иностранные слова (англицизмы) допустимы только если у них нет аналога в русском языке или если это товарный знак.
В рекомендациях приведены примеры некорректного оформления вывесок.
Риски: Штрафы за нарушение требований к языку рекламы и информации для потребителей достигают 500 000 рублей на юрлицо.
Что сделать: Проведите аудит упаковки, инструкций, сайта и интернет-магазина на предмет англицизмов («Sale», «Premium», «Discount», «Medical device»). Русский текст должен быть не менее читаемым, чем иностранный.
Искусственный интеллект в медицине: рамочный законопроект (Минцифры)
Минцифры разработало проект рамочного закона об ИИ (публичное обсуждение до 15 апреля 2026, вступление в силу — 1 сентября 2027 года).
Ключевые определения, которые нужно знать: Искусственный интеллект, Система ИИ, Сервис ИИ, Модель ИИ.
Категории субъектов: Разработчики ИИ-моделей, Операторы ИИ-систем, Владельцы ИИ-сервисов, Пользователи ИИ-сервисов.
Важный нюанс для бизнеса: законопроект предусматривает модель ответственности соразмерно степени вины. Это потребует пересмотра договорных инструментов перераспределения рисков между заказчиками и разработчиками ИИ-решений (например, для диагностических систем на основе ИИ).
Что делать: Если вы разрабатываете или внедряете ИИ-решения в медицине (диагностика, анализ изображений, поддержка принятия решений), уже сейчас закладывайте в договоры гибкие механизмы распределения ответственности.
Смежное: Стратегически значимые лекарства (для держателей РУ, работающих на стыке)
Постановление Правительства от 17 марта 2026 № 277 утвердило правила формирования перечня стратегически значимых лекарственных средств (СЗЛС).
Почему это важно для медизделий: Многие компании имеют портфели и ЛС, и МИ. Кроме того, с 1 июля 2026 вступает в силу механизм «второй лишний» для лекарств из перечня СЗЛС. Если вы работаете с комбинированными терапиями (ЛС + устройство введения), следите за изменениями.
Итоги марта 2026: Чек-лист действий
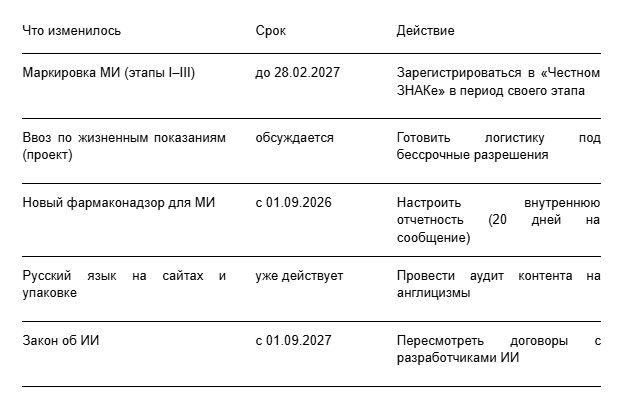
Нужна помощь с адаптацией к новым требованиям? Мы сопровождаем регистрацию и обращение МИ в России. Напишите — разберем вашу ситуацию индивидуально. Просто направьте запрос на почту zapros@regtrend.ru или свяжитесь с нами по телефону +7(495)147-34-57.


